細胞培養進口血清進口胎牛血清進口新生牛血清進口豬血清馬血清
細胞培養進口血清進口胎牛血清進口新生牛血清進口豬血清馬血清 支原體檢測盒及標準品常規PCR檢測試劑盒熒光定量PCR檢測(qPCR法)支原體DNA提取靈敏度標準品(方法驗證用)特異性標準品(方法驗證用)PCR定量標準品(可用于方法驗證)
支原體檢測盒及標準品常規PCR檢測試劑盒熒光定量PCR檢測(qPCR法)支原體DNA提取靈敏度標準品(方法驗證用)特異性標準品(方法驗證用)PCR定量標準品(可用于方法驗證) 支原體祛除試劑細胞中支原體祛除環境支原體祛除水槽支原體祛除
支原體祛除試劑細胞中支原體祛除環境支原體祛除水槽支原體祛除 干細胞培養基
干細胞培養基 DNA/RNA污染祛除DNA/RNA污染祛除試劑DNA污染監測
DNA/RNA污染祛除DNA/RNA污染祛除試劑DNA污染監測 RNA病毒研究試劑RNA病毒檢測試劑盒病毒RNA提取
RNA病毒研究試劑RNA病毒檢測試劑盒病毒RNA提取 PCR儀器及配套產品DNA污染監測祛除PCR/qPCR儀性能檢查PCR試劑PCR試劑盒PCR預混液(凍干粉)熱啟動聚合酶MB Taq DNA
PCR儀器及配套產品DNA污染監測祛除PCR/qPCR儀性能檢查PCR試劑PCR試劑盒PCR預混液(凍干粉)熱啟動聚合酶MB Taq DNA 微生物PCR檢測食品檢測類產品食品微生物檢測細菌PCR檢測
微生物PCR檢測食品檢測類產品食品微生物檢測細菌PCR檢測
- 細胞培養進口血清進口胎牛血清進口新生牛血清進口豬血清馬血清
- 支原體檢測盒及標準品常規PCR檢測試劑盒熒光定量PCR檢測(qPCR法)支原體DNA提取靈敏度標準品(方法驗證用)特異性標準品(方法驗證用)PCR定量標準品(可用于方法驗證)
- 支原體祛除試劑細胞中支原體祛除環境支原體祛除水槽支原體祛除
- 干細胞培養基
- DNA/RNA污染祛除DNA/RNA污染祛除試劑DNA污染監測
- RNA病毒研究試劑RNA病毒檢測試劑盒病毒RNA提取
- PCR儀器及配套產品DNA污染監測祛除PCR/qPCR儀性能檢查PCR試劑PCR試劑盒PCR預混液(凍干粉)熱啟動聚合酶MB Taq DNA
- 微生物PCR檢測食品檢測類產品食品微生物檢測細菌PCR檢測
|
|
協調瞬時基因表達的基礎2018-08-24 13:34來源:締一生物
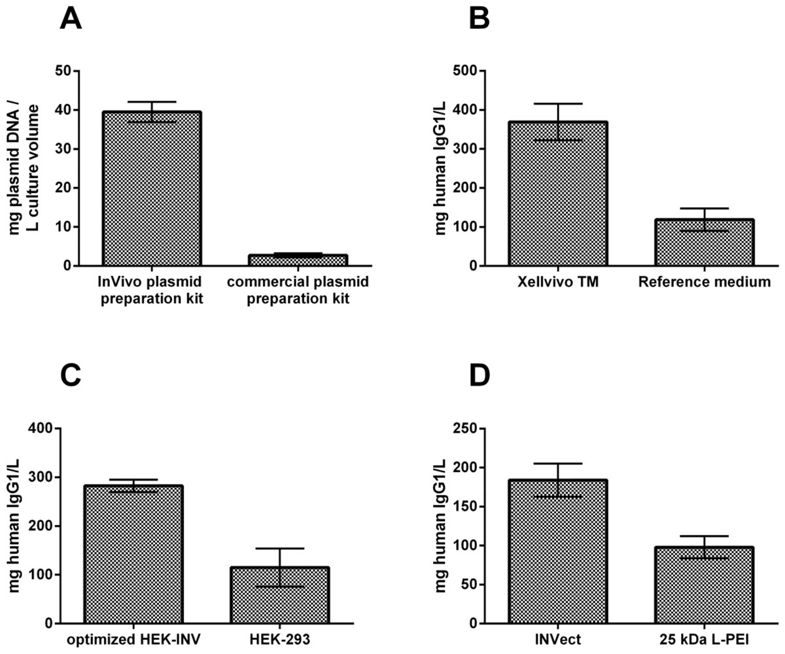
第24屆歐洲動物細胞技術協會(ESACT)會議論文:細胞,培養,患者,產品 題目:協調瞬時基因表達的基礎:從DNA制備(通過培養基、試劑和細胞系開發)到整體工藝優化 文獻出處:BMC Proceedings. 2015, 9 (Suppl 9) https://doi.org/10.1186/1753-6561-9-S9-P18 背景 瞬時基因表達(TGE)有四方面的影響因素:首先,必須有易于轉染的細胞系,能高豐度表達和懸浮培養(1)。其次,鑒于只有少數商品化細胞培養基支持瞬時轉染和表達,強烈建議選擇最合適的培養基(2)。第三,質粒DNA的質量、來源和骨架有重要影響[3]。第四,選擇合適的轉染試劑對于高產起著重要作用。 在這項工作中,我們總結了我們最近開發的一種新型的TGE系統,用于在HEK細胞中進行有效的瞬時轉染和表達。InVivo BioTech Services與emp Biotech公司合作開發了一種極低細胞毒性的轉染試劑,與Xell AG合作設計了可用于轉染和生產的培養基。建立TGE優化的HEK細胞系(HEK-INV)和用于相應載體的大規模質粒制備的方法完善了優化的生產平臺。它易于應用,可擴展,并支持大規模轉染,可在幾天內產生克級的IgG。 材料與方法 哺乳動物細胞在XellvivoTM培養基(貨號861-0001,Xell AG)中培養和轉染,伴隨條件為37℃、5%CO2、185rpm攪拌速度和50mm軌道直徑。轉染方法如下:2μgDNA/細胞+INVect轉染試劑(貨號FK-0101-M001.0-001,emp Biotech GmbH)轉染5×106細胞/ mL,其中INVect與DNA的比例為6:1(w / w);或轉染試劑采用25kDa L-PEI,PEI與DNA比例2:1(w / w),8mL培養液,50mL生物反應管。IgG1的表達分別在125mL轉瓶中的30mL培養液或500mL轉瓶中的150mL培養液中進行,并用蛋白A親和層析定量。定向進化是參考Majors等人2009年的研究[4]進行。具體來說,是進行了數輪的迭代進化,隨后進行了**性狀分析、細胞篩選和細胞回收。相應的流式細胞術分析采用了Bio-Rad S3細胞分選儀。 與微型制備規模的商業試劑盒相比,我們對幾種大腸桿菌菌株和培養基進行了小規模的篩選,以與商品化試劑盒相比,獲得高產、高質和DNA制備的靈活性。采用了可重復使用且可規模升級的陰離子交換器進行純化。對于大規模質粒制備,采用了?ktaprime色譜系統對6L懸浮液進行了裂解、澄清和純化。最后,用DoE軟件和方法對TGE過程進行了優化。 結果 使用在三種不同培養基中培養的,在產量和質量方面比較至少兩種質粒。 對于不同的大腸桿菌菌株,我們比較了三種培養基和至少兩種質粒,評價了質粒產量和質量。在質量方面,超螺旋單體DNA的量高度依賴于宿主菌株,絕對產量則受培養基的影響。采用了陰離子交換法進行了純化。4次獨立的試驗顯示,產量平均為40mg質粒DNA / 每L培養液(圖1A)。 然而,出乎意料的是,高達50,000 EU/ mL的內毒素水平似乎不影響細胞活力、轉染效率,對生產能力也沒有顯著影響。 從哺乳動物培養的基礎培養基開始,我們與Xell AG公司合作,開發了支持瞬時轉染和高滴度表達的新型培養基。通過逐步篩選和優化培養基組分實現了更高的細胞生長,轉染效率和生產能力。最終的培養基配方使IgG1的生產力提高了4倍(圖1B)。 我們利用定向進化,篩選出用于TGE過程的優化的宿主細胞系。與親本宿主細胞系相比,其IgG1的生產力增加了3倍(圖1C)。 常用的轉染試劑如聚乙烯亞胺(PEI)在較高濃度時具有較大的細胞毒性。這使**的可轉染細胞密度受到限制,因為轉染時需要約0.5pgDNA/細胞。要達到類似的生產水平,25kDa L-PEI需要更大的細胞培養容器。新開發的INVect轉染試劑對哺乳動物細胞的瞬時轉染顯示出低細胞毒性,并且具有極高轉染效率,24小時后最高達90%。與25kDa線性PEI相比,INVect轉染后細胞目的蛋白的表達量更高,IgG生產力升高了2倍(圖1D)。
所有開發方面的組合可采取兩種過程策略。一方面,INVect的低毒性和新培養基系統的性能允許在高細胞密度(約1-4x107細胞/ mL)下轉染和培養,實現高達850mg/L的抗體滴度(表1)。另一方面,有可能以高密度(約4x107細胞/ mL)建立**個高產量偽灌注TGE生產過程,這使得每個反應器體積和每天的**空間時間產率高達200mg IgG。 表1. 在具有不同設置和規模的獨立實驗中瞬時表達單克隆抗體
*最終抗體濃度in perfundate 結論 總之,InVivo的TGE系統包括發達的細胞系和載體系統、新型轉染試劑以及獨特的定制培養基,所有這些都協同優化,可高效生產重組蛋白。這種流水線工藝是應用在早期開發階段,下一步即產物鑒定以及臨床試驗前的克級規模生產。 此外,還開發了一種偽灌注TGE方法,用于生產有毒或不穩定的產品,如酶或疫苗。最后,采用了濃縮定制的養料補充劑的生產工藝更簡明,使抗體滴度高達850mg/L。隨后對轉染增強劑的篩選顯示出有希望的結果并表明更進一步改進的潛力。 參考文獻 1. Hacker DL, Kiseljak D, Rajendra Y, Thurnheer S, Baldi L, Wurm FM: Polyethyleneimine-based transient gene expression processes for suspension-adapted HEK-293E and CHO-DG44 cells. Protein Expr Purif. 2013, 92: 67-76. 2. Geisse S: Reflections on more than 10 years of TGE approaches. Protein Expr Purif. 2009, 64: 99-107. 3. Rozkov A, Larsson B, Gillstrom S, Bjornestedt R, Schmidt SR: Large-scale production of endotoxin-free plasmids for transient expression in mammalian cell culture. Biotechnol Bioeng. 2008, 99: 557-566. 4. Majors BS, Chiang GG, Betenbaugh MJ: Protein and Genome Evolution in Mammalian Cells for Biotechnology Applications. Mol Biotechnol. 2009, 42: 216-223. 上一篇: 用于轉染和單細胞培養的化學限定培養基
|
 細胞培養進口血清
細胞培養進口血清 支原體祛除試劑
支原體祛除試劑 干細胞培養基
干細胞培養基